Материал қосу
Химиялық тепе-теңдік
- Химия
- 16.02.2023
- 0
- 0
- 2042
Госплемстанция жалпы орта білім беретін мектебінің химия пәнінің мұғалімі
Джумашева Лаззат Утешовна
|
Ұзақ мерзімді жоспар бөлімі: |
10.2С Химиялық тепе-теңдік |
Мектеп: Госплемстанция жалпы орта білім беретін мектебі |
Теректі ауданы |
|||||||||||||||||||||||||||||||||||||
|
Күні: |
|
Мұғалімнің аты-жөні: |
Л.У.Джумашева |
|||||||||||||||||||||||||||||||||||||
|
Сынып: |
10 |
Қатысқандар саны: 8 |
Қатыспағандар саны: 8 |
|||||||||||||||||||||||||||||||||||||
|
Сабақ тақырыбы |
Химиялық тепе-теңдік |
|||||||||||||||||||||||||||||||||||||||
|
Оқу мақсаттары |
10.3.3.1 химиялық тепе-теңдіктің динамикалық сипатын түсіндіру |
|||||||||||||||||||||||||||||||||||||||
|
Сабақ мақсаттары |
Барлық оқушылар үйренеді: |
|||||||||||||||||||||||||||||||||||||||
|
- Химиялық тепе-теңдіктің динамикалық сипатын түсіну. |
||||||||||||||||||||||||||||||||||||||||
|
Оқушылардың көбісі үйренеді: |
||||||||||||||||||||||||||||||||||||||||
|
- Химиялық тепе-теңдік константасының өрнегін жазу |
||||||||||||||||||||||||||||||||||||||||
|
Кейбір оқушылар үйренеді: |
||||||||||||||||||||||||||||||||||||||||
|
- Химиялық тепе-теңдікке есеп шығару. |
||||||||||||||||||||||||||||||||||||||||
|
Бағалау Критерийлері |
- Химиялық тепе-теңдіктің динамикалық сипатын біледі; - Химиялық тепе-теңдік константасының өрнегін жаза алады; - Химиялық тепе-теңдікке есеп шығара алады. |
|||||||||||||||||||||||||||||||||||||||
|
Тілдік мақсаттар |
Оқушылар: - химиялық тепе-теңдік түсінігін анықтап, айта алады. Пәнге қатысты лексика мен терминология Тепе-теңдік, динамикалық, ұстаным, тұрақты, реагенттер, өнім, температура, қысым, айналмайтын, алға, баяулату, тең, ұлғайту, тепе-теңдік константасы. Диалогқа/жазылымға қажетті тіркестер Егер біз концентрацияны/температураны/қысымды өзгертсек, онда… Біз ... жолымен реакцияны қайтымды ете аламыз Егер температура көтерілсе, онда… Біз осы реакция үшін кері реакция өткізе аламыз ба? Ия, егер біз.… /Жоқ, себебі… Тақырыпқа сәйкес үш тілдік терминдердер тізімі:
|
|||||||||||||||||||||||||||||||||||||||
|
АҚТ қолдану дағдылары |
Презентация |
|||||||||||||||||||||||||||||||||||||||
|
Өмірмен байланысы |
- оқушылардың жас ерекшеліктеріне байланысты жұмыс жасау әдістерімен тәсілдерін қолдану. |
|||||||||||||||||||||||||||||||||||||||
|
Пәнаралық байланыстар |
Физика |
|||||||||||||||||||||||||||||||||||||||
|
Сабақ барысы |
||||||||||||||||||||||||||||||||||||||||
|
Сабақтың жоспарланған кезеңдері |
Сабақтағы жоспарланған іс-әрекет |
Ресурстар |
||||||||||||||||||||||||||||||||||||||
|
Сабақтың басы 2 минут
8-минут |
(W) Ұйымдастыру кезеңі: 1) Оқушылармен амандасу. 2) Оқушыларды түгелдеу. 3) Оқушылардың сабаққа дайындығын тексеру. Өткен тақырыптарды қайталау. Тест. (Google forms) https://forms.gle/raK2GeQih6h5dxoa6 1. 1 моль көміртекте атом саны қанша? A) А. 6,02 ∙ 10²³ В) 6,02²³ С. 6 ∙ 23¹º 2. 10 моль күкірттің массасы (г) – A) 3,2 C) 320 D) 32 A)1 C) 2 D) 3 E) 4 4. Темір атомының ядросындағы протондар саны A) A. 20 C) B. 55 D) 30 E) 8 A) A. 19 г C) 20 D) 30 E) 40 |
https://forms.gle/raK2GeQih6h5dxoa6
|
||||||||||||||||||||||||||||||||||||||
|
Сабақтың ортасы 20-минут |
(W) Жаңатақырыпқа шығу: Мұғалімнің іс-әрекеті. 1. Берілген сурет бойынша сабақ тақырыбын анықтаңыз. Оқушының іс-әрекеті. Суретке қарап, бүінгі тақырыпты анықтайды. Мұғалімнің іс-әрекеті. 2. Химиялық тепе-теңдік туралы видеокөрсетілім көрсетеді. Оқушының іс-әрекеті. Оқушылар видеоролик бойынша өз ойларымен бөліседі. 3. Оқулықпен жұмыс. (Оқушылар оқулықты оқып шығады, жұпта ой бөліседі) Химиялық реакциялар жүру бағытына қарай қайтымды-қайтымсыз реакциялар деп жіктеледі. Қайтымды реакция деп – берілген температурада бір мезгілде өнім түзілу жағына да, бастапқы зат түзілу жағына да жүретін химиялық реакциялар. Тура және кері бағыттағы реакциялар әрі қарай тоқтамай жүре береді, сондықтан тепе-теңдік динамикалық деп аталады. Қайтымды реакцияның тепе-теңдік күйі тепе-теңдік константасымен сипатталады. Мысалы, аА + bB= cC + dD Тапсырма №1. Берілген қайтымды реакциялардың тепе-теңдік константасының өрнегін жазыңдар:
Тапсырма №2. 2-есеп. Егер белгілі бір температурада бастапқы алынған 5 моль СО мен 4 моль Сl2 әрекеттесуі нәтижесінде 1,5 моль СОС12 түзілген болса,онда: СО(г) +Сl2 (г) ↔ COCl2 Процесінің тепе-теңдік константасы қандай болғаны? Шешуі: Химиялық реакция теңдеуі бойынша пропорциялар құрып, реагенттердің реакцияға түскен және артылып қалған мөлшерлерін, сонымен қатар түзілген өнімнің зат мөлшерін тауып, төменгі кестені толтырамыз:
Тепе –теңдік константасы: kтура [COCl2] 1.5 моль/ л К= ———— = ————— = ————————- = 0.17(моль/ л)-1 Kкері [CO] * [Cl2] 3.5 моль/ л* 2.5 моль/ л
|
|
||||||||||||||||||||||||||||||||||||||
|
Сабақтың соңы 5-минут |
Оқушыларға сұрақ. «Миға шабуыл». 1. Химияялық тепе-теңдік деген не? 2. Химиялық тепе-теңдіктің динамикалық деп аталу себебі не? 3. Тепе-теңдік константасы деген не? |
|
||||||||||||||||||||||||||||||||||||||
|
Бағалау 5-минут Үй жұмысы |
Рефлексия. Кері байланыс. Сабақ мақсаттары және бағалау критерийлеріне қайта оралу. Қайталау |
|
||||||||||||||||||||||||||||||||||||||
Пікірлер (0)
Пікір қалдырыңыз
Басқа да жазбалар
- Фосфор қосылыстары
- Табиғаттағы су, құрамы, қасиеттері, қолданылуы
- Жеті сайыс
- Химиядан сабақ жоспары
- Сабақтың технологиялық картасы
- Кремний және оның қосылыстары
- «Бейметалдар мен металдар» тарауына арналған жарыс сабағы
- Табиғаттағы, химиялық реакциялар тірі организмдер мен
- Оттек топшасын қайталау
- Оксидтер. Тотығу. Олардың атаулары
- Химиялық байланыстың негізгі түрлері
- Строение атома
- Кремний және оның қосылыстары
- Аминдер
- Химия ғажайыптары
Бөлімдер
- Кембридж тәсілімен оқыту
- Ана тілі
- Қазақ тілі және әдебиеті
- Орыс тілі және әдебиет
- Ағылшын тілі
- Информатика
- Математика
- Физика
- Химия
- Биология
- География пәні
- Қазақстан тарихы
- Дүние жүзі тарихы
- Құқық негіздері
- Сурет және сызу
- Технология
- Музыка
- Дене шынықтыру
- Алғашқы әскери дайындық
- Мектепалды дайындық
- Бастауыш сынып
- Тәрбие сағаты
- Сауат ашу
- Балабақша
- Өзін-өзі тану
- Әр түрлі
- Ізденіс жұмыстары
- Еңбек
- Экология
- Технология
- Психология
- Экономика

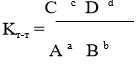
- Азамат Төре (авторлық өңдеу)
- Шәкәрім Құдайбердіұлы
- Азамат Төре
- Абдраманов Арсланбек
Барлық авторлар
Ілмек бойынша іздеу
Мақал-мәтелдер
Қазақша есімдердің тізімі